في المقابل، يُعدّ تاريخ C57BL/6 جيدًا شائعًا لأنه أكثر سلالات البحث غير المستخدمة، وأكثر من أدوات بناء CRISPR التي تُحلل C57BL/6 كجينوم أساسي. يوفر اتحاد تسلسل جينوم الفأر (MGSC) الجديد اقتراحاتٍ لتسلسل جينومي دقيق لبناء الحمض النووي للمتبرع. يجب اختبار موضع أي إدخال مُستهدف بعناية فائقة لتجنب التأثير على أي عوامل تنظيمية. على الرغم من استخدام CRISPR، يصعب إنتاج إدخالات عالية الحجم تزيد عن 5 كيلو بايت في الفئران.
بما في ذلك، لإنشاء أليل ناقض مشروط ممتاز، يمكن لحمض نووي واحد طويل من متبرع SS يحتوي على إكسون/إكسونات مُفلَكة أن يعمل بكفاءة أكبر من مجرد التلاعب بزوج من sgRNAs، مما يسمح بإدخال مواقع loxP. على غرار المتطلبات الفعلية في زيجوت الفأر، سيتم اختبار التعرف على sgRNAs في مجتمع الأنسجة عندما تتوفر أبحاث الكيسة الأريمية للفئران المانحة (ران وآخرون، 2013أ). يمكن استخدام خلايا باريس، مثل (وانغ وآخرون، 2013؛ يانغ وآخرون، 2013) لتحديد نتائج تعديل الجينوم قبل الحقن، لأن خلايا Es تتمتع بكفاءة HDR أفضل من الأنسجة الجسدية (يو وآخرون، 2015).
عوامل الوقت
إلى جانب كفاءة sgRNA، هناك قلق آخر بشأن تعديل الجينوم يتمثل في احتمالية حدوث طفرات من الهدف، خاصةً عند محاولة التعرف على النمط الظاهري للفأر. يوفر برنامج تصميم sgRNA CRIPSR قائمةً بالمواقع المحتملة البعيدة عن الهدف، وبالتالي، عند الإمكان، سيتم تطبيق استراتيجية تعتمد على تفاعل البوليميراز المتسلسل (PCR) لتحديد أي طفرات إندِل في هذه المواقع باستخدام اختبار عدم التطابق الكيميائي. يمكن استخدام التكاثر في فأر بري "نظيف" لفصل الطفرات غير المرغوب فيها (ويفضل إجراء تهجينين على الأقل للتخفيف من طفرات العنوان من الهدف) (Raveux et al., 2017).
2 إنشاء وبناء ركيزة خطية بسبب تفاعل البوليميراز المتسلسل

قد يكون تعديل معايير الإباضة الفائقة وجمع الزيجوت ضروريًا، مع مراعاة الضغوط الأخرى (Qin et al., 2016). يمكن نقل sgRNA وcas9 mRNA إلى الزيجوت الفأري إما عن طريق الحقن السيتوبلازمي، أو باستخدام مُعالج دقيق عالي الجودة قائم على أساس بيزو، أو عن طريق الحقن النووي، وعادةً ما يكون باستخدام مُعالج دقيق عالي الجودة (Yang et al., 2014). بشكل عام، لم تُلاحظ أي اختلافات ظاهرية مع أي نوع من الولادة (Horii et al., 2014).
لتحقيق تعديل الجينوم في أنسجة الثدييات، ستقوم هذه الحذفات بتعطيل جين معين نتيجةً لطفرة تغيير الإطار أ. بدلاً من ذلك مدفوعات كازينو bitcoin ، عند الحصول على الحمض النووي للمتبرع، سيتم تثبيت أحدث DSB مع HDR، حتى لو كان ذلك بتردد أقل من NHEJ. تم تعديل CRISPR-Cas9 لاحقًا للتحكم الوراثي في الحيوانات الكاملة، مما قد يؤدي إلى تعطيل الجين وتعطيله في الفئران.
يمكن استخدام إعادة التركيب أيضًا لإجراء عمليات الحذف، والطفرات الجزئية، والتضاعف، والانعكاسات، والاندماجات، والعلامات. يتم استخدام ركيزة خطية عالية الجودة من الحمض النووي (DNA) تحتوي على التغيير المطلوب أو التماثلات المتماثلة للحمض النووي للعنوان في العضلة. لا يُعد Gam ضروريًا لإعادة التركيب، ولكنه يزيد من انتظام إعادة تركيب الحمض النووي ثنائي السلسلة (dsDNA) حتى 20 انحناء. يُعد Exo نوكليازًا خارجيًا خاصًا بالحمض النووي ثنائي السلسلة (5'→3') ضروريًا لإعادة تركيب الحمض النووي ثنائي السلسلة. يُعد بروتين بيتا الجديد، وهو بروتين تلدين الحمض النووي أحادي السلسلة (ssDNA)، إنزيم إعادة التركيب الرئيسي في عملية إعادة التركيب. والجدير بالذكر أن ميزات إعادة التركيب الرئيسية، مثل بروتين إعادة التركيب السري RecA، ليست ضرورية لإعادة التركيب.
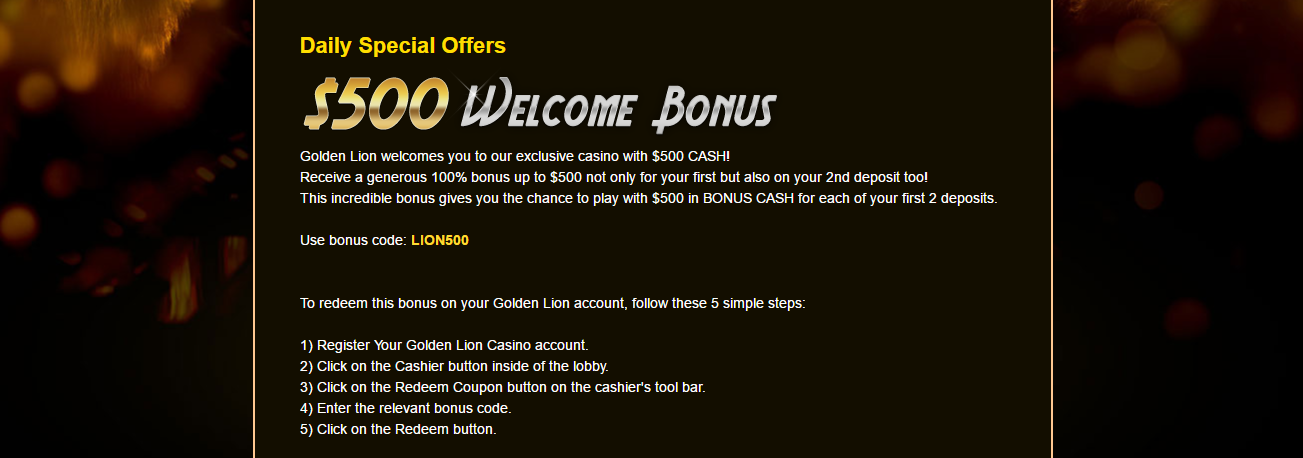
بناءً على خطة موقع loxP، تُنتج عملية إعادة التركيب الجيني الجديدة حذفًا أو انقلابًا لجينات العنوان. ونتيجةً لطبيعة جين cre-loxP القابلة للتحريض، يُحتمل أن تُحفَّز عملية الحذف الجديدة بواسطة مركبات كيميائية مثل التتراسيكلين والتاموكسيفان. يعمل التتراسيكلين على تحفيز نسخ إنزيم cre recombinase الجديد، بينما يتولى التاموكسيفان مسؤولية النقل النووي. تُنشئ البادئات الجانبية منتجًا في المكان الذي يقع فيه الحذف غير المتماثل في أحدث جهاز تفاعل البوليميراز المتسلسل (PCR). يُشق أي عدم تطابق بواسطة إنزيم T7E1 (WT – النوع البري؛ HT – متغاير الزيجوت) لإنتاج شظايا أقصر في هلام الأغاروز.
بينما يُغيّر آل أوليفاريس وضعية جذعهم للدخول في نزال داخلي جديد على يمين كاستيلو، تُشكّل لكمة كاستيلو العلوية إطارًا على شكل حرف A لمنع أوليفاريس من الحصول على ضربة خطافية. ولإعادة ضبط جسده، يُوجّه كاستيلو لكمة علوية قوية لإفساح المجال له ليبدأ نزاله الداخلي، مُعيدًا ضبطه إلى طول مناسب. مع ذلك، عندما لم يتمكن أوليفاريس من دخول النزال الداخلي على جبهتهم المعتادة، تقلّصت قدرته على استخدام لكماته الخطافية المُثبتة بشكل كبير.
بالإضافة إلى عمليات الحذف الأعلى، أثبتت تقنية كريسبر فعالية إدخال جينومات أعلى في عمليات الحذف (تشانغ وآخرون، ٢٠١٥). يُعد حقن جينات sgRNAs التوأمية طريقة مثالية لزيادة فرص استهداف الجين الجديد، خاصةً إذا كان تعديل الجينات ثنائي الأليلات مطلوبًا (تشو وآخرون، ٢٠١٤). وُجدت طفرات غير مستهدفة بشكل عام لتعديل جينوم كريسبر في خلايا سرطان الفرد، ولكنها قد تكون نادرة في زيجوت الفأر (فو وآخرون، ٢٠١٣؛ يانغ وآخرون، ٢٠١٣). ومع ذلك، لا تزال الطفرات غير المستهدفة تُمثل مشكلة عند دراسة الفئران المُعدّلة وراثيًا. يُؤدي قطع واحد من جين Cas9n إلى كسر في الوتر يُمكن إصلاحه بسهولة؛ وبالتالي، لإنشاء DSB أصلي، يلزم وجود جينين sgRNA. تتميز تقنية CRISPR-Cas9 بشكل أساسي باستبدال الجينات التي يتم التركيز عليها داخل أنسجة الخلايا الجذعية الجنينية كوسيلة لتحرير الجينوم داخل الفئران، ويرجع ذلك إلى الإطار البسيط والوقت الأقصر المطلوب للحصول على الفئران المؤسسة.
- نظرًا لأن فريق دوران يتفوق على فريق بالومينو الذي يتصدر الترتيب مباشرة، فإن بالومينو يواجه صعوبة في توجيه ضربة يمينية إلى الصدارة.
- يتم تدمير موقع EcoRI من خلال إدخال الحمض النووي للمتبرع حتى تتمكن من استيعاب النمط الجيني للفأر الذي تم إنشاؤه بواسطة CRISPR والذي لم يتم قطع حلقة KI PCR فيه بسبب Lso.
- على الرغم من أن عمليات الإدراج أو الحذف الأعلى قد لا تتطلب ذلك، إلا أنها قد تتطلب عددًا من sgRNAs لتغطية حجم الحمض النووي الجينومي بالكامل ليتم تغييره أو إزالته.
- تُفضل أنماط الفئران الشرطية على دراسة الوضع البشري لأن بعضها يكشف عن تشابه داخل النمط الظاهري عند إزالة الجينات المحددة.
- تم إجراء إدخالات بحجم 1-2 كيلوبايت فقط باستخدام CRISPR، ولكن النتائج من HDR تتضاءل عمومًا لأن حجم أبعاد الإدخال الأحدث ينمو إلى ما بعد هذا الطول.
بالإضافة إلى سهولة استخدام إنزيم Cas9 في إنزيم نوكلياز الحمض النووي، أُعيد استخدام تقنية كريسبر لإضافة نمطٍ يعتمد على الحمض النووي الريبوزي (RNA) للتحكم في النشاط النسخي الجديد للجينات المستهدفة. يتحقق ذلك باستخدام Cas9 مُعطّل (dCas9) مرتبط بمنشطات النسخ، ومثبطات النسخ، ومعدلات التخلق فوق الجيني (كومور وآخرون، 2017). كبديل، يُمكن أيضًا تفعيل الجينات المستهدفة باستخدام Cas9 من النوع المُكسر من خلال استخدام جزيئات sgRNAs الميتة المُعدّلة والمُكوّنة من أبتامرات MS2 ذات الدبابيس الشعرية. تُقلل جزيئات sgRNAs الميتة هذه لمنع تكوين DSB، لأن أبتامرات MS2 تستخدم بروتين اندماجي يتكون من أحدث بروتين نهاية بكتيريا MS2 المرتبط بمنشط نسخي جيد (لياو وآخرون، 2017). تم إثبات فعالية أسلوب تنشيط الجينات المستهدفة في الفئران في إبعاد التعبير الموجه عن الجينات المعروفة بقدرتها على المساعدة في تحسين الأمراض بما في ذلك مرض السكري، وأمراض الكلى، واعتلال العضلات.

تُسرّع هذه التقنيات الجينية، بالإضافة إلى التطوير النهائي لتقنية CRISPR-Cas9، من وقت نمو الفئران المُعدّلة وراثيًا من 8 إلى 10 أشهر إلى 90 يومًا. مع ذلك، تُقدّم تقنية CRISPR-Cas9 حلولًا جذرية لـ ZFNs وTALENs من حيث الهيكل والبنية (الشكل 1). تتطلب ZFNs وTALENs تجميع نطاقات ربط الحمض النووي متعدد الوحدات لكل هدف جينومي جديد. تعتمد تقنية CRISPR على تكوين ريبونوكليوبروتين مُركّب بين نوكلياز الحمض النووي Cas9 وRNA "الدليلي" الذي يُرسل فيه DSB الجينومي إلى 20 bp من التسلسل الفرعي المُنسّق.
